Кристаллические решетки
Поговорим о твердых телах. Твердые тела можно разделить на две большие группы: аморфные и кристаллические. Разделять мы их будем по принципу есть порядок или нет.
В аморфных веществах молекулы располагаются хаотично. В их пространственном расположении нет никаких закономерностей. По сути, аморфные вещества – это очень вязкие жидкости, настолько вязкие, что твердые.

Отсюда и название: «а-» – отрицательная частица, «morphe» – форма. К аморфным веществам относятся: стекла, смолы, воск, парафин, мыло.
Отсутствие порядка в расположении частиц обусловливает физические свойства аморфных тел: они не имеют фиксированных температур плавления. По мере нагревания их вязкость постепенно снижается, и они также постепенно переходят в жидкое состояние.
В противоположность аморфным веществам существуют кристаллические. Частицы кристаллического вещества пространственно упорядочены. Это правильная структура пространственного расположения частиц в кристаллическом веществе называется кристаллической решеткой.

В отличии от аморфных тел, кристаллические вещества имеют оправленные фиксированные температуры плавления.
В зависимости от того какие частицы находятся в узлах решетки, и от того какие связи удерживают их различают: молекулярную, атомную, ионную и металлическую решетки.
Для чего принципиально важно знать, какая у вещества кристаллическая решетка? Что она определяет? Все. Структура определяет, как химические и физические свойства вещества.
Самый простой пример: ДНК. У всех организмов на земле она построена из одинакового набора структурных компонентов: нуклеотидов четырех видов. А какое многообразие жизни. Это все определяется структурой: порядком, в котором эти нуклеотиды расположены.
Молекулярная кристаллическая решетка.
Типичный пример вода – в твердом состоянии (лед). В узлах решетки находятся целые молекулы. И удерживают их вместе межмолекулярные взаимодействия: водородные связи, силы Ван-дер-Ваальса.

Связи эти слабые, поэтому молекулярная решетка – самая непрочная, температура плавления таких веществ низкая.
Хороший диагностический признак: если вещество имеет при нормальных условиях жидкое или газообразное состояние и/или имеет запах – то скорее всего у этого вещества молекулярная кристаллическая решетка. Ведь жидкое и газообразное состояния – это следствие того, что молекулы на поверхности кристалла плохо держатся (связи то слабые). И их «сдувает». Это свойство называется летучестью. А сдутые молекулы, диффундируя в воздухе доходят до наших органов обоняния, что субъективно ощущается как запах.
Молекулярную кристаллическую решетку имеют:
- Некоторые простые вещества неметаллов: I2, P, S (то есть все неметаллы, у которых не атомная решетка).
- Почти все органические вещества (кроме солей).
- И как уже говорилось ранее, вещества при нормальных условиях жидкие, либо газообразные (будучи замороженными) и/или имеющие запах (NH3, O2, H2O, кислоты, CO2).
Атомная кристаллическая решетка.
В узлах атомной кристаллической решетки, в отличие от молекулярной, располагаются отдельные атомы. Получается, что удерживают решетку ковалентные связи (ведь именно они связывают нейтральные атомы).
Классический пример – эталон прочности твердости – алмаз (по химической природе – это простое вещество углерод). Связи: ковалентные неполярные, так как решетку образуют только атомы углерода.

А вот, например, в кристалле кварца (химическая формула которого SiO2) есть атомы Si и O. Поэтому связи ковалентные полярные.
Физические свойства веществ с атомной кристаллической решеткой:
- прочность, твердость
- высокие температуры плавления (тугоплавкость)
- нелетучие вещества
- нерастворимы (ни в воде, ни в других растворителях)
Все эти свойства обусловлены прочностью ковалентных связей.
Веществ в атомной кристаллической решеткой немного. Особой закономерности нет, поэтому их нужно просто запомнить:
- Аллотропные модификации углерода (C): алмаз, графит.
- Бор (B), кремний (Si), германий (Ge).
- Только две аллотропные модификации фосфора имеют атомную кристаллическую решетку: красный фосфор и черный фосфор. (у белого фосфора – молекулярная кристаллическая решетка).
- SiC – карборунд (карбид кремния).
- BN – нитрид бора.
- Кремнезем, горный хрусталь, кварц, речной песок – все эти вещества имеют состав SiO2.
- Корунд, рубин, сапфир – у этих веществ состав Al2O3.
Наверняка возникает вопрос: С – это и алмаз, и графит. Но они же совершенно разные: графит непрозрачный, пачкает, проводит электрический ток, а алмаз прозрачный, не пачкает и ток не проводит. Отличаются они структурой.

И то, и то – атомная решетка, но разная. Поэтому и свойства разные.
Ионная кристаллическая решетка.
Классический пример: поваренная соль: NaCl. В узлах решетки располагаются отдельные ионы: Na + и Cl – . Удерживает решетку электростатические силы притяжения между ионами («плюс» притягивается к «минусу»), то есть ионная связь.

Ионные кристаллические решетки довольно прочные, но хрупкие, температуры плавления таких веществ довольно высокие (выше, чем у представителей металлической, но ниже чем у веществ с атомной решеткой). Многие растворимы в воде.
С определением ионной кристаллической решетки, как правило, проблем не возникает: там, где ионная связь – там ионная кристаллическая решетка. Это: все соли, оксиды металлов, щелочи (и другие основные гидроксиды).
Металлическая кристаллическая решетка.
Металлическая решетка реализуется в простых веществах металлах. Ранее мы говорили, что все великолепие металлической связи можно понять лишь вместе с металлической кристаллической решеткой. Час настал.
Главное свойство металлов: электроны на внешнем энергетическом уровне плохо удерживаются, поэтому легко отдаются. Потеряв электрон металл превращается в положительно заряженный ион – катион:
В металлической кристаллической решетке постоянно протекают процессы отдачи, и присоединения электронов: от атома металла в одном узле решетки отрывается электрон. Образуется катион. Оторвавшийся электрон притягивается другим катионом (или этим же): вновь образуется нейтральный атом.
В узлах металлической кристаллической решетки находятся как нейтральные атомы, так и катионы металла. А между узлами путешествуют свободные электроны:

Эти свободные электроны называются электронным газом. Именно они обусловливают физические свойства простых веществ металлов:
- тепло- и электропроводность
- металлический блеск
- ковкость, пластичность
Это и есть металлическая связь: катионы металлов притягиваются к нейтральным атомам и все это «склеивают» склеивают свободные электроны.

P.S. Есть кое-что в школьной программе и программе ЕГЭ по этой теме то, с чем мы не совсем согласны. А именно: обобщение, о том, что любая связь металл-неметалл – это ионная связь. Это допущение, намеренно сделано, видимо, для упрощения программы. Но это ведет к искажению. Граница между ионной и ковалентной связью условная. У каждой связи есть свой процент «ионности» и «ковалентности». Связь с малоактивным металлом имеет малый процент «ионности», она больше похожа на ковалентную. Но по программе ЕГЭ, она «округляется» в сторону ионной. Это порождает, порой абсурдные вещи. Например, Al2O3 – вещество с атомной кристаллической решеткой. О какой ионности здесь может идти речь. Только ковалентная связь может удерживать таким образом атомы. Но по стандарту «металл-неметалл» мы квалифицируем эту связь как ионную. И получается противоречие: решетка атомная, а связь ионная. Вот к чему приводит, излишнее упрощение.
himiyaklas.ru
Вещества имеющие металлическую кристаллическую решетку как правило










Вещество, как вам известно, может существовать в трех агрегатных состояниях: газообразном, жидком и твердом. Например, кислород, который при обычных условиях представляет собой газ, при температуре -194 °С превращается в жидкость голубого цвета, я при температуре -218,8º С затвердевает в снегообразную массу, состоящую из кристаллов синего цвета.
В этом параграфе мы рассмотрим, как влияют особенности химических связей на свойства твердых веществ. Температурный интервал существования вещества в твердом состоянии определяется его температурами кипения и плавления. Твердые вещества делятся на кристаллические и аморфные.
Аморфные вещества не имеют четкой температуры плавления — при нагревании они постепенно размягчаются и переходят в текучее состояние. В аморфном состоянии, например, находится пластилин или различные смолы.
Кристаллические вещества характеризуются правильным расположением тех частиц, из которых они состоят: атомов, молекул и ионов. — в строго определенных точках пространства. При соединении этих точек прямыми линиями образуется пространственный каркас, который называют кристаллической решеткой. Точки, в которых размещены частицы кристалла, называют изложи решетки.
В узлах воображаемой решетки могут находиться ионы, атомы и молекулы. Эти частицы совершают колебательные движения. С повышением температуры размах этих колебаний возрастает, что приводит, как правило, к тепловому расширению тел.
В зависимости от типа частиц, расположенных в узлах кристаллической решетки, и характера связи между ними различают четыре типа кристаллических решеток: ионные, атомные, молекулярные и металлические (табл. 6).
Простые вещества остальных элементов, не представленные в таблице 6, имеют металлическую решетку.
Ионными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью, которой могут быть связаны как простые ионы Na+,Сl-, так и сложные SO 2- 4, ОН-. Следовательно, ионные кристаллические решетки имеют соли, некоторые оксиды и гидроксиды металлов, то есть те вещества, в которых существует ионная химическая связь. Например, кристалл хлорида натрия построен из чередующихся положительных ионов Na+ и отрицательных Сl-, образующих решетку в форме куба. Связи между ионами в таком кристалле очень устойчивы. Поэтому вещества с ионной решетной обладают сравнительно высокой твердостью и прочностью, они тугоплавки и нелетучи.
Атомными наливают кристаллические решетки, в узлах которых находятся отдельные атомы. В таких решетках атомы соединены между собой очень прочными ковалентними связями. Примером веществ с таким типом кристаллических решеток может служить алмаз — одно из аллотропных видоизменений углерода.

Число веществ с атомной кристаллической решеткой не очень велико. К ним относятся кристаллические бор, кремний и германий, а также сложные вещества, например такие, в состав которых входит оксид кремния (IV) — SlО2: кремнезем, кварц, песок, горный хрусталь.
Большинство веществ с атомной кристаллической решеткой имеют очень высокие температуры плавления (например, у алмаза она свыше 3500 ºС), они прочны и тверды, практически нерастворимы.
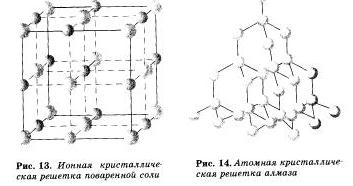
Молекулярными называют кристаллические решетки, в узлах которых располагаются молекулы. Химические связи в этих молекулах могут быть и полярными и неполяриыми. Несмотря на то что атомы внутри молекул связаны очень прочными ковалентными связями, между самими молекулами действуют слабые силы можмолекулярно-го притяжения. Поэтому вещества с молекулярными кристаллическими решетками имеют малую твердость, низкие температуры плавления, летучи.
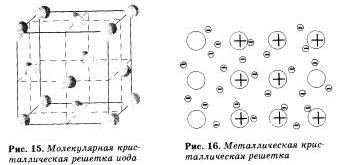
Примерами веществ с молекулярными кристаллическими решетками являются твердая вода — лед, твердый оксид углерода (IV) — «сухой лед», твердые хлороводород и сероводород, твердые простые вещества, образованные одно- (благородные газы), двух- , трех- (О3), четырех- (Р4). восьмиатомными молекулами. Большинство твердых органических соединений имеют молекулярные кристаллические решетки (нафталин, глюкоза, сахар).
Вещества с металлической связью имеют металлические кристаллические решетки. В узлах таких решеток находятся атомы и ионы (то атомы, то ионы, в которые легко превращаются атомы металла, отдавая свои внешние электроны в общее пользование). Такое внутреннее строение металлов определяет их характерные физические свойства: ковкость, пластичность, электро- и теплопроводность, характерный металлический блеск.
Для веществ, имеющих молекулярное строение, справедлив открытый французским химиком Ж. Л. Прустом (1799—1803) закон постоянства состава. В настоящее время этот закон формулируется так: «Молекулярные химические соединения независимо от способа их получения имеют постоянный состав и свойства. Закон Пруста является одним из основных законов химии. Однако для веществ с нсмолекулярным строением, например ионным, этот закон не всегда справедлив.
1. Твердое, жидкое и газообразное состояния вещества.
2. Твердые вещества: аморфные и кристаллические.
3. Кристаллические решетки: атомные, ионные, металлические и молекулярные.
4. Закон постоянства состава.
Какие свойства нафталина лежат в основе его применения для защиты шерстяных изделий от моли?
Какие качества аморфных тел применимы для опнсаиия особенностей характера отдельных людей?
Почему открытый датским ученым К. X. Эрстедом алюминий в 1825 г. еще долгое время относился к драгоценным металлам?
Вспомните произведение А. Беляева «Продавец воздуха» и охарактеризуйте свойства твердого кислорода, используя его описание, приведенное в книге.
Почему температура плавления металлов изменяется в очень широких пределах? Для подготовки ответа на этот вопрос используйте дополнительную литературу.
Почему изделие из кремния при ударе раскалывается на кусочки, а изделие из свинца только расплющивается? В каком из указанных случаев происходит разрушение химической связи, а в каком — нет? Почему?
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь — Образовательный форум.
edufuture.biz
Тест по химии (8 класс) по теме:
Тестирование по теме «Кристаллические решётки веществ»

Тестирование для проверки знаний учащихся и подготовке по теме «Кристаллические решётки веществ»
Предварительный просмотр:
Вариант 1 Тест: « Типы кристаллических решёток»
1.В узлах разных кристаллических решеток могут находиться
1.Атомы 2. Электроны 3.Протоны
2.Выберите вещества, имеющие атомную кристаллическую решетку.
2.Сульфат меди 4.Оксид кремния
3.Выберите вещества, имеющие ионную кристаллическую решетку:
1. оксид кремния 2.хлорид натрия 3.гидроксид калия 4.сульфат алюминия
4.Атомная кристаллическая решётка характерна для:
a). алюминия и графита б). серы и йода
в). оксида кремния и хлорида натрия г). алмаза и бора
5) Изотопами являются:
а). этан и этен б). О 16 и О 17
в). натрий и калий г). графит и азот
6) Вещества, имеющие металлическуюую кристаллическую решётку, как правило:
a). тугоплавки и хорошо растворимы в воде
б). легкоплавки и летучи
в). Тверды и электропроводны
г). Теплопроводны и пластичны
8. Какой тип кристаллической решётки у следующих широко используемых в быту веществ: 1.вода, 2.уксусная кислота (CH 3 COOH), 3.сахар (C 12 H 22 O 11 ), 4.алмаз? Сделайте обобщённый вывод: по каким свойствам вещества можно определить тип его кристаллической решётки?
9 По формулам приведённых веществ: NaBr, C 2 H 2 — определите тип кристаллической решётки (ионная, молекулярная) каждого соединения и на основе этого опишите физические свойства каждого из четырёх веществ.
10.выберите признаки характерные для веществ с молекулярнойой кристаллической решёткой:
- В узлах кристаллической решётки находятся нейтральные атомы
- Это летучие вещества
- Основным агрегатным состоянием — является твердое состояние вещества
- Это тугоплавкие вещества
- В узлах кристаллической решётки находятся полярные и неполярные молекулы
- Частицы в узлах кристаллической решетке связаны друг с другом ковалентной связью
- Данные вещества не растворяются в воде
- Это ковкие и пластичные вещества
- В узлах кристаллической решётки находятся положительные и отрицательные ионы
- Это твёрдые и прочные вещества
- Это непрочные вещества
- Частицы в узлах кристаллической решетке связаны друг с другом ионной связью
- Эти вещества имеют металлический блеск
- В узлах кристаллической решётки находятся нейтральные атомы и положительные ионы металла
- Частицы в узлах кристаллической решетке связаны друг с другом силами межмолекулярного взаимодействия
- Представителями являются соли
- Представителями являются простые вещества неметаллы, в обычном состоянии являющиеся газами
- Данные вещества хорошо растворяются в воде
- Растворимость этих веществ зависит от полярности химической связи
- Данные вещества имеют низкую температуру кипения
- Частицы в узлах кристаллической решетке связаны друг с другом металлической связью
- Представителями являются твердые, тугоплавкие неметаллы
- Данные вещества способны проводить электрический ток
Вариант 2 Тест: « Типы кристаллических решёток»
1 .Среди перечисленных веществ выберите вещества, которые имеют кристаллическое строение.
1.воск 2.алмаз 3.каменная соль 4.»сухой лед»
2 .В узлах разных кристаллических решеток могут находиться
1.атомы 2.электроны 3.протоны 4.ионы 5.молекулы
3. Аллотропией называется:
1. существование для атомов одного и того же элемента нескольких устойчивых изотопов
2. способность атомов элемента образовывать несколько сложных веществ с атомами другого элемента
3. существование нескольких сложных веществ, молекулы которых имеют одинаковый состав, но различное химическое строение
4. существование нескольких простых веществ, образованных атомами одного и того же элемента
5) Если вещество хорошо растворимо в воде, имеет высокую температуру плавления, электропроводно, то его кристаллическая решётка:
а). молекулярная б). атомная
в). ионная г). металлическая
6) Вещества, имеющие молекулярную кристаллическую решётку, как правило:
a). тугоплавки и хорошо растворимы в воде
б). легкоплавки и летучи в). Тверды и электропроводны
7. Какой тип кристаллической решётки у следующих широко используемых в быту веществ: 1.калийное удобрение (KCl), 2.речной песок (SiO 2 ) – температура плавления 1710 0 C, 3.аммиак (NH 3 ), 4.поваренная соль? Сделайте обобщённый вывод: по каким свойствам вещества можно определить тип его кристаллической решётки?
8 По формулам приведённых веществ: SiC, CS 2 — определите тип кристаллической решётки (ионная, молекулярная) каждого соединения и на основе этого опишите физические свойства каждого из четырёх веществ.
9.выберите признаки характерные для веществ с ионной кристаллической решёткой:
- В узлах кристаллической решётки находятся нейтральные атомы
- Это летучие вещества
- Основным агрегатным состоянием — является твердое состояние вещества
- Это тугоплавкие вещества
- В узлах кристаллической решётки находятся полярные и неполярные молекулы
- Частицы в узлах кристаллической решетке связаны друг с другом ковалентной связью
- Данные вещества не растворяются в воде
- Это ковкие и пластичные вещества
- В узлах кристаллической решётки находятся положительные и отрицательные ионы
- Это твёрдые и прочные вещества
- Это непрочные вещества
- Частицы в узлах кристаллической решетке связаны друг с другом ионной связью
- Эти вещества имеют металлический блеск
- В узлах кристаллической решётки находятся нейтральные атомы и положительные ионы металла
- Частицы в узлах кристаллической решетке связаны друг с другом силами межмолекулярного взаимодействия
- Представителями являются соли
- Представителями являются простые вещества неметаллы, в обычном состоянии являющиеся газами
- Данные вещества хорошо растворяются в воде
- Растворимость этих веществ зависит от полярности химической связи
- Данные вещества имеют низкую температуру кипения
- Частицы в узлах кристаллической решетке связаны друг с другом металлической связью
- Представителями являются твердые, тугоплавкие неметаллы
- Данные вещества способны проводить электрический ток
nsportal.ru
Кристаллические решетки в химии
Содержание:
Определение кристаллической решетки
Как мы знаем, все материальные вещества могут пребывать в трех базовых состояниях: жидком, твердом, и газообразном. Правда есть еще состояние плазмы, которое ученые считают ни много ни мало четвертым состоянием вещества, но наша статья не о плазме. Твердое состояние вещества потому твердое, так как имеет особую кристаллическую структуру, частицы которой находятся в определенном и четко заданном порядке, создавая, таким образом, кристаллическую решетку. Строение кристаллической решетки состоит из повторяющихся одинаковых элементарных ячеек: атомов, молекул, ионов, других элементарных частиц, связанных между собой различными узлами.
Виды кристаллических решеток
В зависимости от частиц кристаллической решетки существует четырнадцать типов оной, приведем наиболее популярные из них:
- Ионная кристаллическая решетка.
- Атомная кристаллическая решетка.
- Молекулярная кристаллическая решетка.
- Металлическая кристаллическая решетка.
Далее более подробно опишем все типы кристаллической решетки.
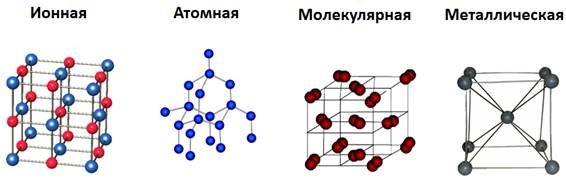
Ионная кристаллическая решетка
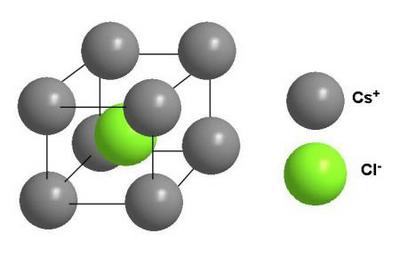
Главной особенностью строения кристаллической решетки ионов являются противоположные электрические заряды, собственно, ионов, вследствие чего образуется электромагнитное поле, определяющее свойства веществ, имеющих ионную кристаллическую решетку. А это тугоплавкость, твердость, плотность и возможность проводить электрический ток. Характерным примером ионной кристаллической решетки может быть поваренная соль.
Атомная кристаллическая решетка
Вещества с атомной кристаллической решеткой, как правило, имеют в своих узлах, состоящих собственно из атомов сильные ковалентные связи. Ковалентная связь происходит, когда два одинаковых атома делятся друг с другом по-братски электронами, образуя, таким образом, общую пару электронов для соседних атомов. Из-за этого ковалентные связи сильно и равномерно связывают атомы в строгом порядке – пожалуй, это самая характерная черта строения атомной кристаллической решетки. Химические элементы с подобными связями могут похвастаться своей твердостью, высокой температурой плавления. Атомную кристаллическую решетку имеют такие химические элементы как алмаз, кремний, германий, бор.
Молекулярная кристаллическая решетка
Молекулярный тип кристаллической решетки характеризуется наличием устойчивых и плотноупакованных молекул. Они располагаются в узлах кристаллической решетки. В этих узлах они удерживаются такими себе вандервальсовыми силами, которые в десять раз слабее сил ионного взаимодействия. Ярким примером молекулярной кристаллической решетки является лед – твердое вещество, имеющее однако свойство переходить в жидкое – связи между молекулами кристаллической решетки совсем слабенькие.
Металлическая кристаллическая решетка
Тип связи металлической кристаллической решетки гибче и пластичнее ионной, хотя внешне они весьма похожи. Отличительной особенностью ее является наличие положительно заряженных катионов (ионов метала) в узлах решетки. Между узлами живут электроны, участвующие в создании электрического поля, эти электроны еще называются электрическим газом. Наличие такой структуры металлической кристаллической решетки объясняет ее свойства: механическую прочность, тепло и электропроводность, плавкость.
Кристаллические решетки, видео
И в завершение подробное видео пояснения о свойствах кристаллических решеток.
www.poznavayka.org
Типы кристаллических решеток
Презентация к уроку
Внимание! Предварительный просмотр слайдов используется исключительно в ознакомительных целях и может не давать представления о всех возможностях презентации. Если вас заинтересовала данная работа, пожалуйста, загрузите полную версию.
Тип урока: Комбинированный.
Цель урока: Создать условия для формирования умения учащихся устанавливать причинно-следственную зависимость физических свойств веществ от вида химической связи и типа кристаллической решетки, предсказывать тип кристаллической решетки на основе физических свойств вещества.
Задачи урока:
- Сформировать понятия о кристаллическом и аморфном состоянии твердых тел, ознакомить учащихся с различными типами кристаллических решеток, установить зависимость физических свойств кристалла от характера химической связи в кристалле и типа кристаллической решетки, дать учащимся основные представления о влиянии природы химической связи и типов кристаллических решеток на свойства вещества.
- Продолжить формирование мировоззрения учащихся, рассмотреть взаимное влияние компонентов целого-структурных частиц веществ, в результате которого появляются новые свойства, воспитывать умения организовать свой учебный труд, соблюдать правила работы в коллективе.
- Развивать познавательный интерес школьников, используя проблемные ситуации;
Оборудование: Периодическая система Д.И. Менделеева, коллекция «Металлы», неметаллы: сера, графит, красный фосфор, кристаллический кремний, йод; Презентация «Типы кристаллических решёток», модели кристаллических решеток разных типов (поваренной соли, алмаза и графита, углекислого газа и йода, металлов), образцы пластмасс и изделий из них, стекло, пластилин, компьютер, проектор.
Ход урока
1. Организационный момент.
Учитель приветствует учеников, фиксирует отсутствующих.
2. Проверка знаний по темам” Химическая связь. Степень окисления”.
Самостоятельная работа (15 минут)
3. Изучение нового материала.
Учитель озвучивает тему урока и цель урока. (Слайд 1,2)
Учащиеся записывают в тетради дату, тему урок.
Актуализация знаний.
Учитель задаёт вопросы классу:
- Какие виды частиц вы знаете? Имеют ли заряды ионы, атомы и молекулы?
- Какие виды химических связей вы знаете?
- Какие вам известны агрегатные состояния веществ?
Учитель: «Любое вещество может быть газом, жидкостью и твёрдым веществом. Например, вода. При обычных условиях – это жидкость, но она может быть паром и льдом. Или кислород при обычных условиях представляет собой газ, при температуре -1940 C он превращается в жидкость голубого цвета, а при температуре -218,8°C затвердевает в снегообразную массу, состоящую из кристаллов синего цвета. На этом уроке мы рассмотрим твёрдое состояние веществ: аморфное и кристаллическое». (Слайд 3)
Учитель: аморфные вещества не имеют чёткой температуры плавления – при нагревании они постепенно размягчаются и переходят в текучее состояние. К аморфным веществам относят, например шоколад, который тает и в руках и во рту; жевательную резинку, пластилин, воск, пластмассы (показываются примеры таких веществ). (Слайд 7)
Кристаллические вещества имеют чёткую температуру плавления и, главное, характеризуются правильным расположением частиц в строго определенных точках пространства. (Слайды 5,6) При соединении этих точек прямыми линиями образуется пространственный каркас, называемый кристаллической решёткой. Точки, в которых размещены частицы кристалла, называют узлами решётки.
Учащиеся записывают в тетрадь определение: «Кристаллической решёткой называют совокупность точек пространства, в которых располагаются частицы, образующие кристалл. Точки, в которых размещаются частицы кристалла, называют узлами решётки».
В зависимости от того, какие виды частиц находятся в узлах этой решётки, различают 4 типа решёток. (Слайд 8) Если в узлах кристаллической решётки находятся ионы, то такая решётка называется ионной.
Учитель задаёт учащимся вопросы:
– Как будут называться кристаллические решётки, в узлах которых находятся атомы, молекулы?
Но есть кристаллические решётки, в узлах которых находятся и атомы, и ионы. Такие решётки называются металлическими.
Сейчас мы будем заполнять таблицу: «Кристаллические решётки, вид связи и свойства веществ». В ходе заполнения таблицы мы будем устанавливать взаимосвязь между типом решётки, видом связи между частицами и физическими свойствами твёрдых веществ.
Далее на экране появляется таблица. (Слайд 9). Её заполнение идёт в ходе диалога учителя с учащимися.
Рассмотрим 1-й тип кристаллической решётки, которая называется ионной. (Слайд 9)
– Какие частицы располагаются в узлах этой решётки?
– Какая химическая связь в этих веществах?
Посмотрите на ионную кристаллическую решётку (показывается модель такой решётки). В её узлах находятся положительно и отрицательно заряженные ионы. Например, кристалл хлорида натрия построен из положительных ионов натрия и отрицательных хлорид-ионов, образующих решётку в форме куба. К веществам с ионной кристаллической решёткой относятся соли, оксиды и гидроксиды типичных металлов. Вещества с ионной кристаллической решёткой обладают высокой твёрдостью и прочностью, они тугоплавкие и нелетучие.
Учитель: Физические свойства веществ с атомной кристаллической решёткой те же, что и у веществ с ионной кристаллической решёткой, но часто в превосходной степени – очень твёрдые, очень прочные. Алмаз, у которого атомная кристаллическая решётка – самое твёрдое вещество из всех природных веществ. Он служит эталоном твёрдости, которая по 10-бальной системе оценивается высшим баллом 10.(Слайд 10). По этому типу кристаллической решётки вы сами внесёте необходимые сведения в таблицу, самостоятельно поработав с учебником.
Учитель: Рассмотрим 3-й тип кристаллической решётки, которая называется металлической. (Слайды 11,12) В узлах такой решётки находятся атомы и ионы, между которыми свободно перемещаются электроны, связывая их в единое целое.
Далее учащиеся по учебнику рассматривают модель металлической кристаллической решётки.
Такое внутреннее строение металлов и определяет их характерные физические свойства.
Учитель: Какие физические свойства металлов вы знаете? (ковкость, пластичность, электро- и теплопроводность, металлический блеск).
Учитель: На какие группы делятся все вещества по строению? (Слайд 12)
Рассмотрим тип кристаллической решётки, которой обладают такие хорошо известные нам вещества как вода, углекислый газ, кислород, азот и другие. Она называется молекулярной. (Слайд14)
– Какие частицы располагаются в узлах этой решётки?
Далее учащиеся по учебнику рассматривают модель молекулярной кристаллической решётки.
Химическая связь в молекулах, которые находятся в узлах решётки, может быть и ковалентная полярная, и ковалентная неполярная. Несмотря на то, что атомы внутри молекулы связаны очень прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного притяжения. Поэтому вещества с молекулярной кристаллической решёткой имеют малую твердость, низкие температуры плавления и летучие. Когда газообразные или жидкие вещества при особых условиях превращаются в твёрдые, тогда у них появляется молекулярная кристаллическая решётка. Примерами таких веществ может быть твёрдая вода – лёд, твёрдый углекислый газ – сухой лёд. Такую решётку имеет нафталин, который применяют для защиты шерстяных изделий от моли.
– Какими свойствами молекулярной кристаллической решётки обусловлено применение нафталина? (летучестью). Как видим, молекулярную кристаллическую решетку могут иметь не только твердые простые вещества: благородные газы, H2,O2, N2, I2, O3, белый фосфор Р4, но и сложные: твердая вода, твердые хлороводород и сероводород. Большинство твердых органических соединений имеют молекулярные кристаллические решетки (нафталин, глюкоза,сахар).
В узлах решеток находятся неполярные или полярные молекулы. Несмотря на то, что атомы внутри молекул связаны прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного взаимодействия.
Вывод: Вещества непрочные, имеют малую твердость, низкую температуру плавления, летучи.
Вопрос: Какой процесс называется возгонкой или сублимацией?
Ответ: Переход вещества из твердого агрегатного состояния сразу в газообразное, минуя жидкое, называется возгонкой или сублимацией.
Демонстрация опыта: возгонка йода
Потом учащиеся по очереди называют сведения, которые они записали в таблицу.
Кристаллические решетки, вид связи и свойства веществ.
xn--i1abbnckbmcl9fb.xn--p1ai